

Les périodes de sécheresse gagnent en fréquence et en intensité, poussant les distributeurs d’eau à diversifier leurs ressources. Cet exercice n’est pas sans risque. Chaque eau naturelle, de par son historique hydrogéologique, a atteint un équilibre chimique. En revanche, lorsque deux eaux de natures différentes sont combinées artificiellement, il est possible de créer une eau déséquilibrée chimiquement.
Un cas typique, fréquent en Suisse, est celui du réseau intercommunal du SIDERE (Service intercommunal de distribution d’eau potable de Rolle et environs), qui est détaillé dans cet article. Le mélange d’eaux de surface et des ressources karstiques peut engendrer une eau corrosive pour le réseau de distribution si celui-ci est constitué de conduites métalliques. A la sortie des réservoirs, cette eau est parfaitement potable selon les normes suisses. Durant son parcours toutefois, l’eau distribuée s’enrichit en fer, à des teneurs pouvant dépasser les normes. Bien que ce phénomène ne cause en général pas de problème pour la santé, il constitue souvent une expérience désagréable pour le consommateur: l’eau distribuée a une coloration jaune-orange et peut avoir un goût métallique prononcé. Des métaux lourds peuvent également être libérés par corrosion. Dans d’autres pays où le plomb est encore présent dans les réseaux d’eau potable, la corrosion de ce métal peut avoir des effets plus sévères sur la santé.
La chimie des eaux naturelles comprend un ensemble de phénomènes complexes et un nombre important d’espèces ioniques. Pour la problématique de l’eau rouge, cette complexité peut être simplifiée à un espace à deux dimensions dont les axes qualifient deux indices chimiques: la corrosivité et l’agressivité, décrits dans les sections suivantes [1].
Toute eau en soit est corrosive et va favoriser l’oxydation du fer élémentaire présent dans les conduites en hydroxyde de fer. Cette oxydation est principalement causée par l’oxygène dissous et produit du fer ferreux (Fe2+) qui est ensuite en grande partie oxydé en fer ferrique (Fe3+) dans une eau naturelle suffisamment oxygénée, puis précipite sous forme d’hydroxydes (Fe[OH]3).
Si l’eau contient des ions sulfates ou des ions chlorures, ceux-ci vont accélérer la corrosion. En revanche, les ions hydrogénocarbonate (HCO3–) auront un effet inverse. L’indice de Larson, pertinent pour décrire la corrosivité d’une eau, est un indice empirique défini par l’équation 1:
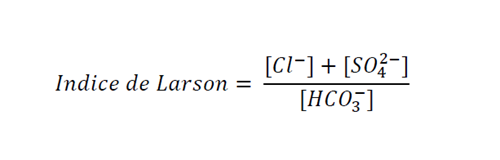
Eq. 1 L'indice de Larson, pertinent pour décrire la corrosivité d'une eau.
Selon l’indice calculé, les eaux peuvent être classées de la manière suivante:
La deuxième notion chimique importante est l’agressivité de l’eau, liée à l’équilibre calco-carbonique. Ce paramètre est bien connu des distributeurs d’eau. En effet, il est recommandé de distribuer une eau proche de l’équilibre afin d’éviter des désagréments tels que la formation de tartre ou la corrosion de conduites. Toutefois, la législation suisse ne spécifie aucune valeur limite pour ce paramètre.
Historiquement, plusieurs méthodes ont été développées pour décrire l’équilibre calco-carbonique des eaux: notamment des méthodes d’approximation basées sur des abaques et des calculs simples (p. ex. Hallopeau-Dubin et l’indice de Langelier). Depuis, des méthodes basées sur des calculs rigoureux d’équilibres chimiques à l’aide de logiciels (p. ex. PHREEQC et LPLWin) ont été développées. Elles permettent de calculer précisément l’équilibre calco-carbonique à partir de la composition chimique de l’eau par le saturatio, un indice qui compare les concentrations en calcium et carbonates avec celles correspondant à l’équilibre, selon l’équation 2:
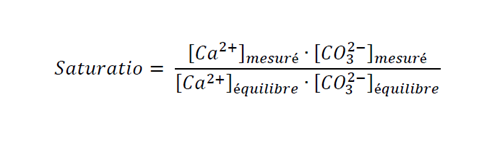
Eq. 2 Calcul du saturatio, un indice qui compare les concentrations en calcium et carbonates avec celles correspondant à l’équilibre.
Toute eau peut être classée dans une de ces trois catégories:
Le saturatio de l’eau joue un rôle primordial pour le contrôle de la corrosion. Si l’eau est suffisamment entartrante, du carbonate de calcaire se dépose sur les parties internes des conduites, formant ainsi une couche de protection qui bloque la corrosion.
Il est possible de tirer parti de ce phénomène. S’il est difficile de rendre une eau moins corrosive en diminuant les concentrations en sulfates et chlorures, il est plus facile d’en modifier le saturatio pour la rendre plus entartrante. Ceci peut être réalisé en augmentant le pH de l’eau par l’ajout d’une base (NaOH), par l’ajout de carbonates (avec du NaHCO3), ou par le retrait d’un acide, tel que le CO2 dissous. Plus une eau est corrosive, et plus il faut la rendre entartrante afin que la vitesse de corrosion soit contrecarrée par la vitesse de formation des carbonates qui vont protéger les conduites.
En réalité, il est souhaitable d’ajouter une 3ème dimension pour considérer cette problématique dans sa globalité. Le réseau de distribution y joue un rôle essentiel, de par sa structure, son historique, sa dynamique, et de par les matériaux composant les conduites. Une bonne connaissance du réseau est nécessaire pour comprendre où, quand et comment des eaux de natures différentes peuvent se mélanger, pour comprendre comment l’équilibre chimique varie dans le réseau, pour déterminer quelles parties du réseau sont sensibles aux problèmes de corrosion, et enfin pour définir à quels endroits il est souhaitable de déployer une solution de traitement.
Le SIDERE distribue 1,6 millions de m3 d’eau par an, à l’aide de 165 km de conduites, à 16'500 habitants répartis sur 12 communes. 55% de l’eau provient du lac Léman (traitement par filtration), et 22 sources karstiques fournissent le solde. Le réseau de distribution est complexe, avec 17 réservoirs et 15 stations de pompage.
Le SIDERE a connu des épisodes d’eau rouge qui ont fait l’objet d’études. Il est intéressant de les détailler ici car cette situation n’est pas du tout un cas particulier. Elle touche de nombreuses autres collectivités suisses, distribuant également des mélanges d’eaux de lacs et d’eaux de sources. Ces mélanges se réalisent soit dans le réseau directement, soit dans des réservoirs, et peuvent ainsi engendrer des eaux rouges. Ces études ont par ailleurs permis au SIDERE d’implémenter une solution performante pour répondre à cette problématique.
Des échantillonnages et des analyses chimiques ont été réalisés sur plusieurs types d’eaux: des eaux de sources, des eaux de réservoirs, des eaux distribuées. Le choix des points de prélèvement a été guidé par la structure du réseau et par des mesures de conductivité qui ont permis de déterminer où les mélanges se réalisent (dans les réservoirs ou directement dans le réseau) et à quels taux.
La détermination de l’équilibre calco-carbonique d’échantillons d’eaux est délicate. Ce paramètre peut être influencé par un dégazage entre l’échantillonnage et les analyses en laboratoire. De plus, une petite erreur sur la mesure de pH peut grandement influencer le saturatio calculé. De ce fait, les pH ont été mesurés directement sur site, à la pression du point d’échantillonnage. Ces mesures ont également été complétées par des mesures sur site de CO2 dissous. Ces analyses ont permis de décrire finement l’évolution du saturatio des eaux de sources au fil de l’eau.
Il est possible de classer les différentes eaux présentes sur le réseau selon leur saturatio et leur indice de Larson (fig. 1). Afin d’éviter les problèmes de corrosion, une eau ne doit pas se situer dans le rectangle rouge, qui correspond à une zone corrosive et agressive.
La principale ressource en eau du SIDERE est le lac Léman. Cette eau est douce (env. 14 °f) et corrosive en raison de concentrations importantes en sulfate et chlorure. Cette eau est également agressive, ayant une tendance à dissoudre les carbonates de calcium. De ce fait, elle fait l’objet d’un traitement classique d’augmentation de saturatio, par ajout de soude. Ceci rend l’eau du lac légèrement entartrante, bloquant les phénomènes de corrosion. Dans le réseau, l’eau du lac traitée dépose une couche de carbonate sur les conduites. Ainsi, le saturatio peut diminuer lors du transport (fig. 1).
La deuxième ressource du SIDERE est constituée des eaux de sources qui proviennent du relief jurassien et dont le débit varie au fil des saisons. Les eaux de source sont généralement dures à très dures (de 25 à 40 °f, riches en calcium), peu corrosives (car pauvres en sulfates et chlorures) mais agressives. Ceci s’explique par de fortes concentrations en CO2 dissous, un acide faible. Le long du réseau, ces eaux deviennent légèrement entartrantes par deux mécanismes: principalement par un léger dégazage dans les réservoirs, mais également par augmentation de la température dans le réseau de distribution (fig. 1).
Ces deux eaux, considérées séparément, sont entartrantes lorsqu’elles sont distribuées dans le réseau. En revanche, lorsqu’elles se rencontrent, soit dans des réservoirs, soit directement dans le réseau, le mélange produit devient agressif, ce qui peut engendrer de l’eau rouge.
Il est possible de modéliser la composition chimique du mélange pour différentes proportions des deux ressources (fig. 2). L’indice de Larson (indice de corrosivité; eq. 1) évolue linéairement en fonction des proportions du mélange. Le mélange de deux eaux peu corrosives produit toujours une eau peu corrosive. En revanche, la situation est différente pour l’équilibre calco-carbonique. Deux eaux, chacune ayant un saturatio > 1 (donc entartrante; eq. 2), peuvent produire un mélange avec un saturatio < 1 (donc agressif). Ainsi, un mélange de deux eaux entartrantes peut devenir agressif et très rapidement dissoudre la couche de tartre qui protégeait les conduites, les rendant ainsi vulnérables à la corrosion.
En fonction de la variabilité des débits des eaux de sources et de la demande, le mélange eau de sources – eau du lac peut survenir à différents endroits dans le réseau de distribution. Des analyses réalisées sur les eaux prélevées dans les réservoirs et dans les conduites du SIDERE ont mis ce phénomène en évidence (fig. 3).
Sur la partie droite du graphique, les eaux constituées uniquement d’eau de lac forment une ligne verticale, avec un saturatio variable. Ceci s’explique par le fait que, une fois une eau entartrante distribuée, elle va déposer une couche de carbonate de calcium durant son parcours, diminuant ainsi ses teneurs résiduelles en carbonates et en calcium et donc son saturatio. Sur la gauche du graphique, les eaux composées uniquement d’eau de source ont également des saturatios variables, en raison d’un dégazage ou d’une augmentation de température. Finalement, la zone de corrosivité intermédiaire (indice de Larson > 0,25 et < 0,7) montre des mélanges mesurés dans le réseau. On voit que le saturatio est plus bas pour certains de ces mélanges. Pour deux échantillons qui ont un indice de Larson proche de 0,6 (classés comme corrosifs), le saturatio est inférieur à 1, ce qui les classe comme agressifs. Ils sont constitués d’eau de lac mélangée à une petite proportion d’eau de source (env. 20%), rendant l’eau agressive et corrosive. Ces deux échantillons correspondent spatialement et temporellement à l’observation d’eaux rouges sur le réseau du SIDERE.
Finalement, en croisant les compositions chimiques des eaux, la structure du réseau avec les données temporelles des débits des ressources, il a été possible de modéliser l’évolution temporelle du saturatio et de l’indice de Larson à différents points du réseau. Cet exercice a permis de mettre en évidence les zones du réseau les plus vulnérables aux problèmes de mélange d’eau, de tester virtuellement l’effet de différents traitements de correction de l’équilibre et de définir des zones-clés où il serait judicieux de traiter l’eau. La figure 4 compare à titre d’exemple une simulation réalisée pour la partie est du réseau du SIDERE d’un traitement de dégazage avec la situation d’origine.
En mélangeant différents types de ressource dans un réseau de distribution, des mélanges d’eau peuvent créer des déséquilibres, tels que des phénomènes de corrosion. Il existe plusieurs solutions techniques à cette problématique. Un adoucissement de l’eau du lac pour y enlever spécifiquement les sulfates peut rendre l’eau moins corrosive. Une rénovation du réseau de distribution pour remplacer toutes les conduites métalliques résoudrait également le problème. Finalement, une correction de l’équilibre calco-carbonique permet de bloquer la corrosion en formant une couche protectrice de tartre. Cette dernière solution est plus simple et plus économique à mettre en œuvre.
L’eau peut être rendue plus entartrante par plusieurs méthodes, par exemple par ajout d’un réactif chimique augmentant les concentrations en calcium ou le pH. Puisque les eaux de sources sont sursaturées en CO2, un gaz dissous qui est également un acide faible, il est possible d’augmenter son pH et son saturatio en extrayant le CO2, sans utiliser de réactif chimique (fig. 5). Plusieurs technologies de dégazage du CO2 existent, tels que des chutes d’eau et des systèmes de ruissellement (si de faibles taux de dégazage sont suffisants), ou des tours de dégazage, des aérateurs à lit plat et des contacteurs membranaires (pour des taux plus élevés et/ou variables).
Pour traiter les eaux de source du SIDERE, des contacteurs membranaires ont été utilisés. Un contacteur est pourvu d’une membrane poreuse et hydrophobe, ne laissant passer que les composés gazeux. D’un côté de la membrane circule l’eau à dégazer, de l’autre côté circule un flux d’air qui va servir à extraire le CO2, entraîné par une soufflante. Parce que la pression partielle de CO2 est plus grande du côté de l’eau, celle-ci va perdre son CO2 au travers de la membrane. Ces contacteurs sont fournis par 3M (LiquiCel) dans un format très compact. Un carter occupant un espace d’environ 0,1 m3 contient environ 220 m2 de surface d’échange (fig. 6).
Cette solution permet de contrôler finement le taux de dégazage. Une sonde pH ou de CO2 située en aval de la membrane peut être utilisée pour contrôler le débit d’air de la soufflante. Plus le flux d’air est important, plus la différence de pression partielle de CO2 entre eau et air est importante et plus le dégazage est important.
Cette solution permet de dégazer de façon efficace, contrôlée et réactive, tout en limitant l’empreinte au sol. Elle permet d’ajuster instantanément le taux de dégazage à la variabilité de la qualité de l’eau ou de la consigne désirée.
Un dégazage par contacteur membranaire a été implémenté au réservoir de Bursins, sur l’entrée des sources du réseau ouest du SIDERE (fig. 7). Le saturatio est réglé de façon à ce que tout mélange avec les eaux de lac produise une eau légèrement entartrante. Le pH des eaux de source passant de 7,35 à 7,80 par dégazage, une couche de tartre peut se former lentement sur les parois internes des conduites du réseau, les protégeant de la corrosion.
L’abattement de CO2 en fonction du débit d’eau et de la fréquence de la soufflante d’air reproduit les résultats des simulations (fig. 8). La relation entre le pH et le saturatio mesurés en sortie de membrane est également conforme aux attentes: plus le pH cible est élevé, plus le dégazage et le saturatio sont élevés (fig. 9). En revanche, il est à noter qu’une faible erreur dans la mesure du pH peut engendrer une forte variation du saturatio. Une dérive d’une sonde pH peut affecter les performances de traitement. Il paraît plus robuste de contrôler ce procédé à l’aide d’une sonde CO2 qui offre l’avantage d’être plus précise et plus stable.
L’installation de dégazage a été mise en service sur les sources du réseau ouest du SIDERE en avril 2020, alors que le traitement par soude de l’eau du lac était en place depuis avril 2019. Le caractère entartant des eaux traitées a été validé par des analyses et les plaintes de consommateurs concernant les problèmes d’eau rouge ont depuis disparu.
La chimie de l’eau est parfois surprenante. Deux eaux de natures différentes, ne causant aucun problème individuellement, peuvent provoquer de la corrosion une fois mélangées. Cette problématique se rencontre régulièrement sur l’arc lémanique, lorsque les eaux de source sont mélangées aux eaux de lac. Pour y remédier, plusieurs solutions existent. Il est bien sûr possible de remplacer toutes les conduites en fonte du réseau, y compris les introductions privées, par des nouvelles conduites non-métalliques.
L’alternative choisie et implémentée par le SIDERE, et décrite dans le présent article, apparait comme plus simple et économique. Suite à une étude détaillée de la corrosivité et de l’agressivité des différentes eaux tout au long de l’année, et de leur taux variable de mélange, une solution a pu être mise en place. Elle consiste en un traitement conjugué de l’eau de lac, par ajout de soude, et de l’eau des sources, par dégazage. Ce dernier traitement est novateur, et est réalisé à l’aide de contacteurs membranaires permettant une désacidification régulée des eaux de sources, par dégazage du CO2. Cette solution permet une distribution d’eau qui reste potable et de qualité sur l’ensemble du réseau en tout temps.
Les défis liés à la crise climatique forcent inévitablement les distributeurs d’eau à diversifier leurs ressources, et la problématique des mélanges d’eau va sans doute prendre de l’ampleur. Dans cette optique, il est primordial que l’ensemble des acteurs de l’eau soit conscient que tout mélange d’eau peut apporter un déséquilibre, avec parfois son lot de désagréments pour le consommateur. Différentes solutions techniques, performantes et économiques, permettent toutefois de les éliminer.
[1] Leroy, P. (2012): Corrosivité des eaux, critères de protection des ouvrages par le carbonate de calcium. European journal of water quality 43(2): 75–78. https://doi.org/10.1051/wqual/2013010
Nous remercions chaleureusement Messieurs Armand Jeanmonod et Thierry Cuénod du SIDERE, ainsi que Messieurs Samuel Grossenbacher et Marc Dvorak du bureau Herter & Wiesmann, pour leur soutien et leur confiance. Nous remercions également Monsieur Pierre Leroy pour son soutien concernant les aspects techniques du projet, notamment les aspects en lien avec la corrosion et l’équilibre calco-carbonique de l’eau.
Avec l'abonnement en ligne, lisez le E-paper «AQUA & GAS» sur l'ordinateur, au téléphone et sur la tablette.
Avec l'abonnement en ligne, lisez le E-paper «Wasserspiegel» sur l'ordinateur, au téléphone et sur la tablette.
Kommentare (0)